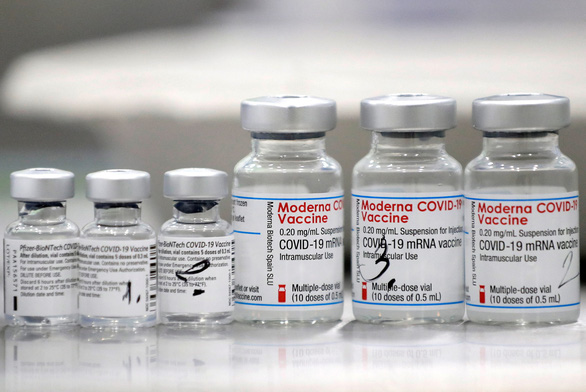
Vaccine cải biến của Pfizer và Moderna có thể ngừa các dòng phụ đang phổ biến của biến thể Omicron - Ảnh: REUTERS
Theo Hãng tin Reuters, cả 2 loại vaccine mới của Pfizer và Moderna đều là vắc xin "lưỡng trị", vì nó không chỉ nhắm vào chủng virus SARS-CoV-2 ban đầu mà còn nhằm vào biến thể Omicron.
Vaccine của Moderna được cấp phép cho người từ 18 tuổi trở lên, trong khi của Pfizer được cấp phép cho người trên 12 tuổi.
Các vaccine thế hệ trước tuy vẫn có thể ngăn ngừa bệnh nặng do COVID-19, nhưng khả năng chống lây nhiễm thấp khi đối diện với ngày càng nhiều biến chủng mới.
Thế hệ vaccine mới này được kỳ vọng sẽ ngăn ngừa tốt việc lây truyền của các dòng phụ như BA.5 Omicron, bên cạnh ngăn ngừa bệnh nặng.
Công ty công nghệ sinh học Moderna cho biết liều tăng cường 50 microgam tạo ra "phản ứng kháng thể vượt trội chống lại biến thể Omicron trong vòng 1 tháng sau khi sử dụng", so với vaccine ban đầu.
Chính phủ Mỹ đã mua 175 triệu liều vaccine tăng cường trong nỗ lực ngăn chặn một đợt lây nhiễm mới khi các trường học mở cửa trở lại và mọi người sẽ ở trong không gian kín nhiều hơn vì mùa đông đã tới gần.
Pfizer cho biết họ có sẵn thuốc để xuất xưởng ngay lập tức và có thể cung cấp tới 15 triệu liều thuốc cho tới ngày 9/9.
Tháng 6 vừa qua, FDA đề nghị các nhà sản xuất vaccine cải biến mũi tăng cường để nhắm mục tiêu vào 2 biến thể dòng phụ đang gây ra làn sóng lây nhiễm gần đây trên khắp thế giới. Biến thể BA.5 hiện chiếm hơn 88% số ca nhiễm tại Mỹ.
Ủy ban cố vấn vaccine của Trung tâm Phòng ngừa và kiểm soát dịch bệnh Mỹ (CDC) dự kiến họp ngày 1/9 để đưa ra khuyến nghị sử dụng các mũi tăng cường nâng cấp nói trên.
Giám đốc CDC Rochelle Walensky sẽ nghiên cứu khuyến nghị này trước khi đưa ra quyết định cuối cùng. Nếu cả FDA và CDC đều bật đèn xanh cho các mũi tiêm mới, 2 loại vaccine này có thể được tiêm trong thời gian sớm nhất.
Theo Tuoitre